 脂肪酸の定義
脂肪酸の定義
←Dataは飛魚をクリック!元来、脂肪を分解して得られた酸性の物質という意味であったように思う。これを化学の用語で表現すると、ある程度の長さの炭化水素鎖があって、酸の性質を示すカルボキシル基が付いたものということになろう。
しかし、様々な例外を考えなければならない。ミコール酸のような超長鎖脂肪酸は脂肪(トリアシルグリセロール)の成分というにははばかられるので、脂肪の分解より得られるというように言い換えねばならないし、リン脂質を分解するとDAFなどでは酢酸が出てくる。酢酸やプロピオン酸は構造的には一連の物質であるが、脂肪酸というには抵抗がある。
結局、炭化水素鎖の一端にカルボキシル基を有し(カルボン酸)水に溶けないものという定義になるのではないだろうか。勿論、生体物質にはジカルボン酸トリカルボン酸があるが、水に溶けない程の炭素鎖を持つジカルボン酸やトリカルボン酸は、天然物としても脂質成分としても見当たらない。
また、酸性基もカルボキシル基とは限らず、硫酸基やリン酸基あるいはフェノール性水酸基など有り得るが、天然物には無いようである。
炭化水素鎖部分も直鎖構造とは限らず分枝構造や環状構造もある。
そして更に炭化水素鎖が水酸基やアミノ基で修飾されると物理化学的性質が大きく変わって全体として水溶性を示す場合も出てくる。因みに、胆汁酸やプロスタグランジン群は炭化水素部分が環状構造であり水酸基を有している。コール酸やPL
2α炭素数は多いが、僅かに水に溶ける。胆汁酸やプロスタノイドは無理に脂肪酸の中で扱うのではなく、別に一括して考えた方が良いと思う。
脂肪酸の溶解度(1)
脂質が水に溶けないという性質を持つのは、構成成分に脂肪酸を有しているからである。勿論、水に溶けないという性質を脂肪酸が結合する長鎖アルコールや長鎖塩基も寄与している事があっても、基本的には脂肪酸の性質に負うところが大きい。
表1. 脂肪酸の水に対する溶解度| C1~C4 | 水に溶ける |
| C5 | 3.1g/100ml |
| C6 | 1.082g/100ml |
| C7 | 2.419g/100ml |
| C8 | 0.068g/100ml |
| C9 | 実際上不溶 |
溶けるとはどういう現象かという定義も難しい問題であるが、とにかくMerck Index等に出てくる水に対する溶解度をまとめてみると、表1のようになる。この表の中で溶ける溶けないの線をどこで引くかの論理はないが、中鎖脂肪酸という言葉にC8,C10,C12が含められることを考えれば、C7とC8の間で線を引くのも一つの方法であろう。短鎖脂肪酸という言葉があるのかどうかわからないが、若しあるとすれば、水とは自由に混ざり合わないC5,C6,C7になるのかもしれない。C4以下はカルボン酸ということになるのであろうか。
脂肪酸の溶解度(2)
①脂肪酸のアルカリ金属塩
脂肪酸のNa-塩、K-塩はいわゆる石鹸として日常生活にあっていつも接触するものである。
遊離状の長鎖、中鎖脂肪酸は事実上水には全く溶けないがNa、K のアルカリ金属塩は水に溶けるようになる。しかし、ある濃度以上になると水分子の間に分散することは不可能で、カルボキシル基を外にしたミセルを形成する。(図1)この濃度を臨界ミセル濃度という。(表2)
表2 臨界ミセル濃度 | g or mg/dl | mmol/l |
C7H15COONa
C7H15COOK
(オクタン酸Na,K) | 6.0g
7.1g | 360(20℃)
390(25℃) |
C9H19COONa
(デカン酸Na) | 1.84~1.94g | 95~100(20℃) |
C12H25COOK
(ドデカン酸K) | 315mg | 12.5(25℃) |
C13H27COONa
C13H27COOK
(ミリスチン酸Na,K) | 175mg
191mg | 7(17~8℃)
7.2 |
C17H35COOK
(ステアリン酸K) | 16mg | 6.5(60℃) |
C17H33COOK
(オレイン酸K) | 48mg | 1.5(25℃) |
C17H33COOK
(エライジン酸K) | 48mg | 1.5(50℃) |
逆に言うと、臨界ミセル濃度以下のオレイン酸カリは分子状で水に分散していることになる。ミセルの形状には球状、環状など様々なものがあるが、ミセルが形成されるようになると、光が散乱して白濁してくる。理論的には、ミセルが形成され始めると、水中の分子状の脂肪酸塩濃度はミセルになった分だけ下がり、水系は脂肪酸塩を溶かし込む能力を回復する。そうすると、脂肪酸塩は更に水に溶け込む一方、次々にミセルが形成される状態になる。つまり脂肪酸塩は水系に溶けてはミセル化し、最終的にはこれだけの溶媒(水)にはこれ以上のミセルは存在し得ないという状態、即ち大量の脂肪酸ミセルの間に少量の水が薄い膜状に存在するという状態になるのではあるまいか。
②金属石鹸
脂肪酸はNa、K のアルカリ金属以外の金属とも塩を作る。これを金属石鹸という。
マグネシウム、カルシウム、亜鉛、アルミニウム、鉛、クロム、モリブデン、タングステン、マンガン、鉄、コバルトなどの塩がよく調べられているが、殆ど水不溶性である。石鹸(脂肪酸のアルカリ金属塩)水溶液に上記の金属の無機塩(塩化物、硫酸塩など)を加えると複分解を起こし水に溶けない金属石鹸が析出してくる。石鹸を硬水で使用すると不溶性の金属塩が析出して使いにくい。
脂肪酸の融点
(動物の)生体膜は柔軟性があり流動性がある。それを支えるのは膜リン脂質とコレステロールの物理化学的性質であり、その基本的性質は構成脂肪酸の融点である。
脂肪酸の融点と炭化水素鎖長
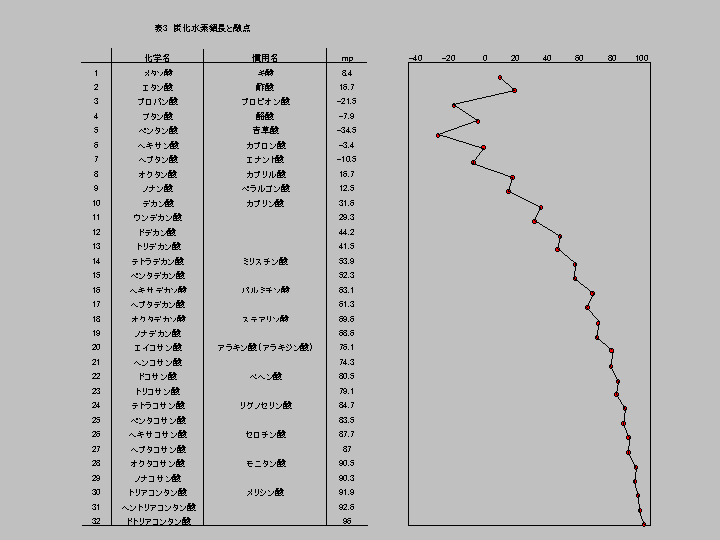
表2にはカルボン酸も入れてあるが、面白いことに奇数酸はその前後の偶数酸より若干低い値を示し、図示したようにギザギザの線になる。しかし、炭素数が30以上になるとそのような現象は見られない。
(表3)
脂肪酸の融点と二重結合-①-位置
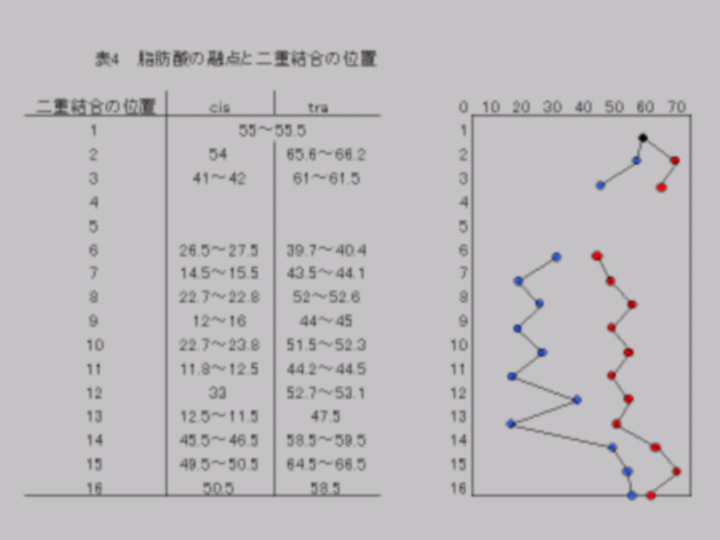
炭化水素鎖に二重結合(不飽和結合)があれば融点が低くなり液状を呈することはよく知られているが、因みにstearic acidは固体酸、oleic acidは油酸と翻訳されていた。炭素数18のモノエン酸について二重結合の位置とその融点をまとめた。(表4)ここにも融点のギザギザが表れている。
* 二重結合の位置はω端(メチル端)から数えて記入した。例えば、8はC8とC9の間に二重結合があるという意味である。従って、16はC16とC17の間に二重結合があるが、C18はカルボキシル炭素であるのでC17C18の間には二重結合を置くことができない。
脂肪酸の融点と二重結合-②-数
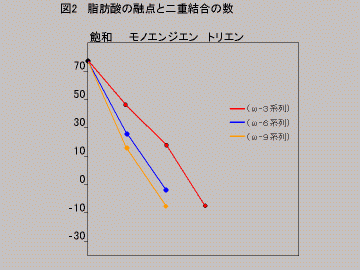
当然二重結合が多くなると融点が低くなり常温で液状になる。また、同じ二重結合酸でも、二重結合の位置によって融点は異なる。(図2)
脂肪酸の融点とメチル側鎖の位置
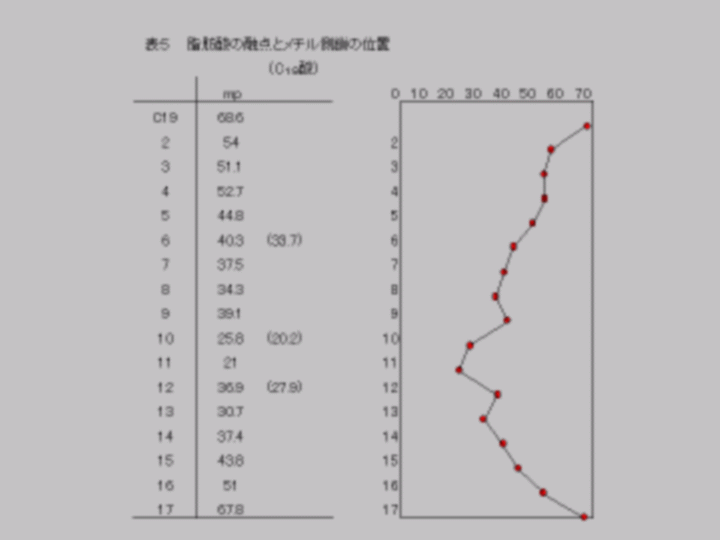
直鎖部分をC18とし、それに1個のメチル基を側鎖として導入してみるとω-11、ω-12辺りが最も融点が低くなる。(表5)
共役二重結合を持つ脂肪酸
我々の体を構成する脂質の高度不飽和脂肪酸、また主な食品脂質の高度不飽和脂肪酸は二重結合と二重結合の間にメチレン基が挿入された非共役二重結合構造であることは周知のことである。
しかし植物界には限られた量、また限られた種類ではあるが不飽和酸がある。桐油は(Tung oil)はアブラギリの種子を圧搾して得られる乾性油でワニスやペイントあるいは、桐油紙、桐油布など防水用材として用いられた。そのトリアシルグリセロールの構成脂肪酸は表6の通りである。
18:3(conj)は一般名エレオステアリン酸(eleostearic acid)()β型は全てがE(trans)form、α型はカルボキシル基側の一つだけがZ(cis)formで、他のE、Z異性体もある。常温では固体である。ほぼ同じヨウ素価を示すアマニ油に比べても桐油の方が速乾性である。
他の植物油にも共役のOctadecatrienoic acidの存在が記載されているしまた、共役のOcta
decatetraennoic acidの記載もある。
共役二重結合を有するポリエン酸の過酸化の様式は非共役二重結合とは異なり外側の二重結合部分に脱水素が起こり酸素が導入される。同じ程度にリノレン酸(非共役Octadeactrienoic acid)を含むアマニ油より速乾性(重合性が高い)である事を考えると共役酸の方が(過)酸化され易いと推定される。
表6.| 16:0 | 3 |
| 18:0 | 2 |
| 18:1 | 11 |
| 18:2 | 15 |
| 18:3(conj) | 69 |
二重結合が連続(Allene構造)する脂肪酸
一般名バレン酸(Laballenic acid)シソ科の植物の種子に広く見出されている二つの二重結合のπ電子の軌道面が直交するため不斉炭素がなくても光学活性(α20/D3.0°)である。
このアレン構造以外に二重結合を持つものもある。




 脂肪酸の定義
脂肪酸の定義