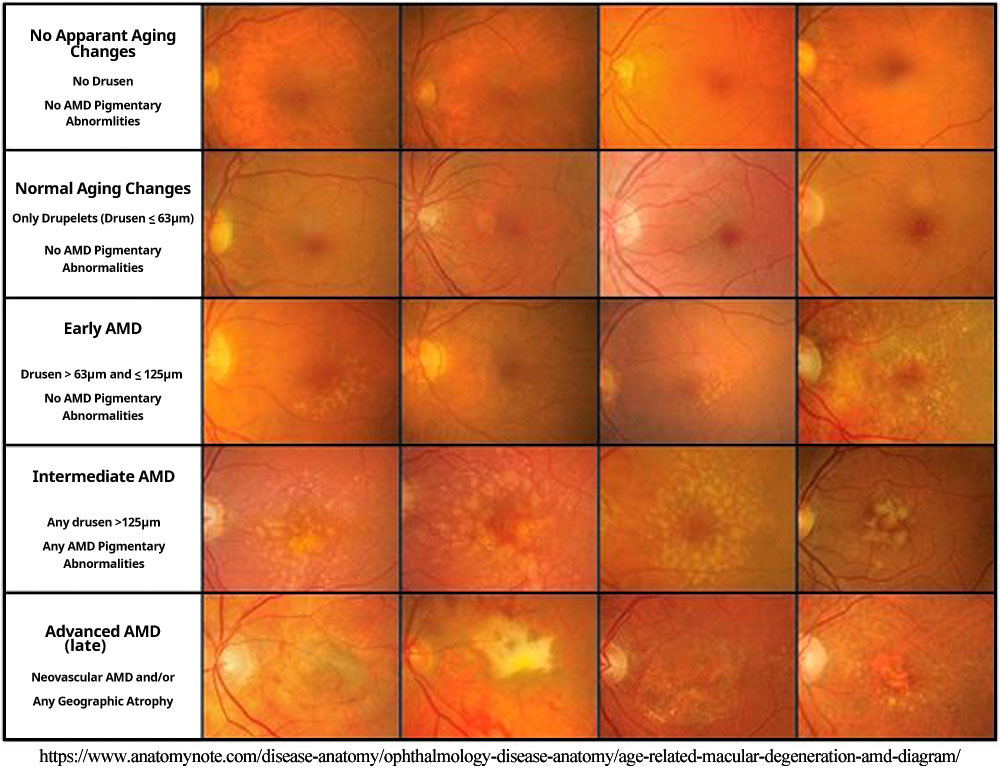
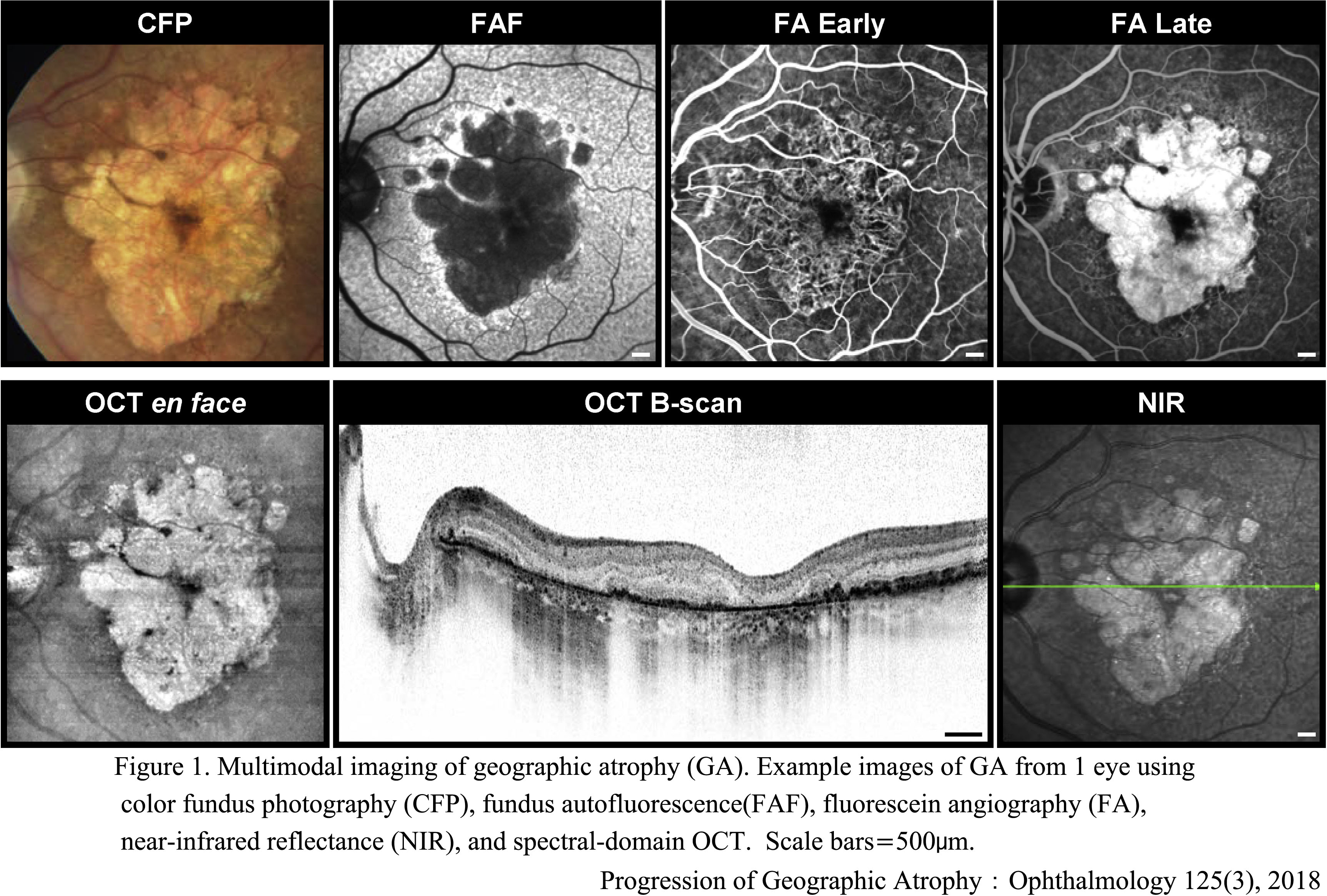
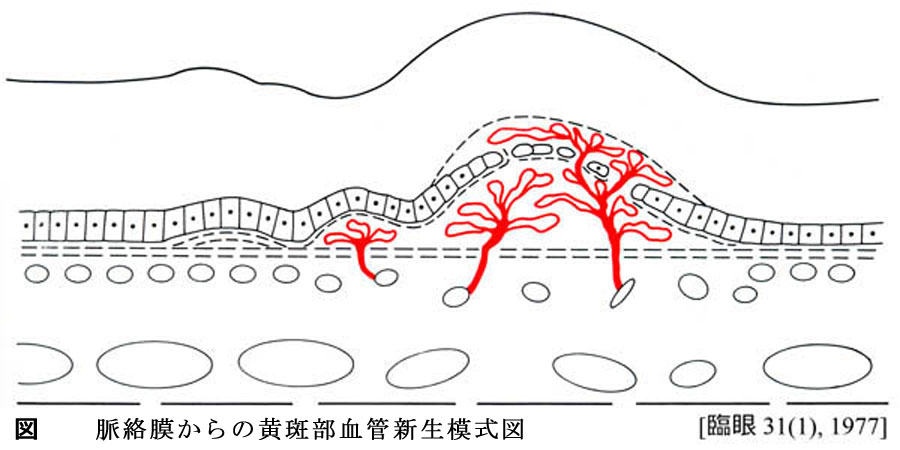
主に50代以上で問題になる,老化に基づく黄斑異常の総称である.視細胞外節-網膜色素上皮層あるいは網膜色素上皮層-Bruch膜への代謝物の沈着・蓄積(extracellular deposit)により,血管新生や組織萎縮をきたす.
加齢変化と云えども基盤には遺伝的要因があり,環境要因の修飾によって発症する.
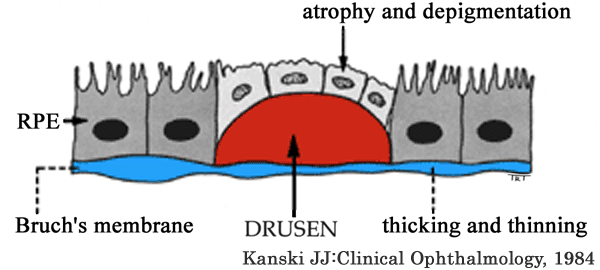
- 加齢黄斑症
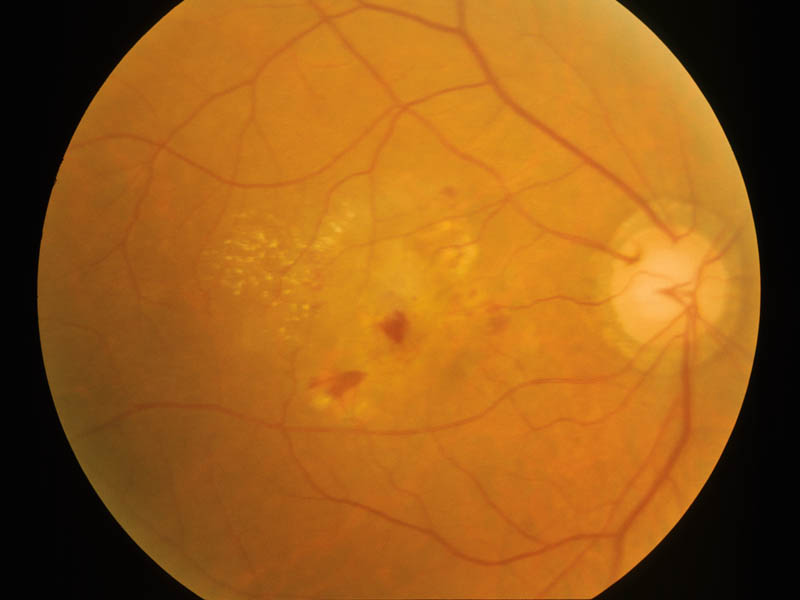
初期加齢黄斑症 early ageⲻrelated maculopathy は軟性ドルーゼンや網膜色素上皮異常を指す,視機能障害を伴わない段階(前駆病変)である.
❶ 網膜色素上皮細胞の変化:網膜色素上皮細胞 RPE は,加齢に伴って細胞質内に リポフスチン顆粒 が増加しメラニン顆粒は減少する.加齢の基本変化(退行変性)である.消化能の低下した色素上皮細胞は,貪食した変性残渣物質を放出する.顆粒を放出すると色素上皮細胞自体は萎縮・崩壊する.視細胞外節も影響を受ける.
網膜色素上皮の異常には,色素脱失,色素沈着,色素ムラに加え小型(1乳頭径未満)の漿液性網膜色素上皮剝離が含まれる.色素脱失とは, 境界不鮮明で脈絡膜血管が透見できない程度のRPEの萎縮と定義されている.色素異常はBruch膜の慢性炎症と見做す.
☆マイクログリアは外節残渣を貪食する.マイクログリアの遊走は炎症状態を生じると指摘されている.❷ ドルーゼン drusen:軟性ドルーゼンに蓄積したAGEsがマクロファージなど炎症細胞の遊走・浸潤を誘導し,慢性炎症が持続する.酸化環境ではマクロファージの老化を招き,老化したマクロファージの中にドルーゼンの主成分であるリポフスチンが蓄積し、網膜下ドルーゼノイド沈着の原因ともなる.
軟性ドルーゼンが1個以上みられれば前駆病変と診断される.
☆AGEs (advanced glycation end products):蛋白糖化最終産物.通常の加齢産物であるが,血管基底膜の肥厚や白血球粘着能の亢進,血液網膜関門の破壊などをきたす元.
☆reticular pseudodrusen:網膜下にドルーゼン様の多形性の debris が沈着したもの(subⲻretinal drusenoid debris)で,AMD,特にRAPの前段階として注目されている. 【 reticular pseudodrusen 】
☆cuticular(basal laminar)drusen:Bruch膜の肥厚した内側が結節様に突出したもので,CNVあるいは偽卵黄様剝離(pseudovitelliform macular detachment lesion)を合併しやすい. 【 basal laminar drusen 】
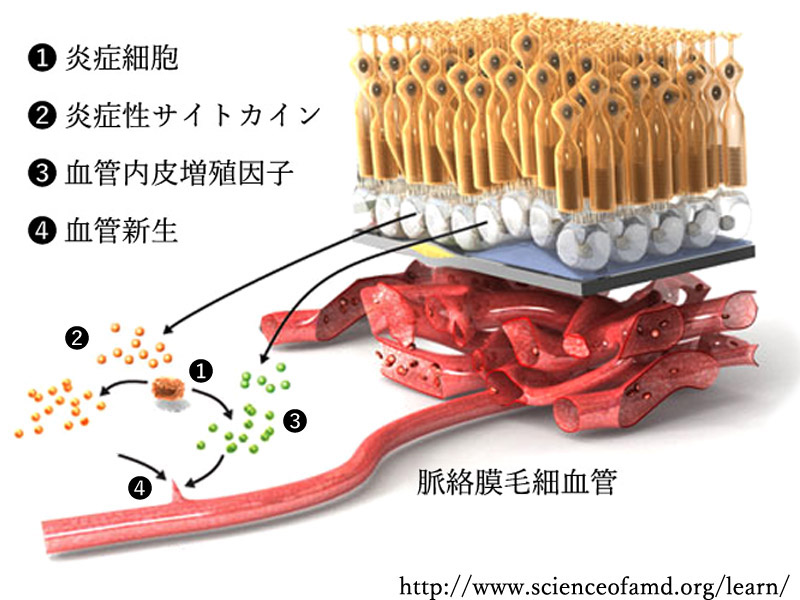
❸ 炎症:蓄積物内には補体成分が証明され,マクロファージが遊走することで慢性炎症状態となる.蓄積物の貪食・排除のための異物反応といわれる.これによりVEGF等が過剰に発現し透過性亢進のほか,脈絡膜血管内皮細胞・線維芽細胞・網膜色素上皮細胞の増殖・線維成分の産生を促がすことになる.即ち 血管新生である.
☆新生血管の発生が網膜外層から起きることがあり,『脈絡膜新生血管』との表現は用いず,macular neovascularization (MNV) との推奨がある.ただし一般には,血管内皮細胞の発芽はおもに脈絡膜の細静脈からである.❹ 網膜色素上皮剝離(retinal pigmentepithelial detachment:PED):沈着脂質が多い軟性ドルーゼンが元になると解釈され,色素上皮基底膜と内膠原線維層のあいだで起こる.新生血管発生の基盤になるのは大型の剝離とされる.
❺ Bruch膜:軟性ドルーゼンとも関連し,一般に肥厚する.脈絡毛細管板のメンテナンスに当たるVEGFがBruch膜を通過しにくくなるため,脈絡毛細管板が萎縮し血管新生の下地になる.
❻ VEGF:血管内皮増殖因子( 血管新生因子 ∕ サイトカイン)は色素上皮から脈絡膜へ放出されている.生理活性の範囲では,網膜・脈絡膜の維持に必要成分である.
☆黄斑部は,感光物質が激しく代謝され温度上昇も加わり,おそらく 酸化ストレス によりVEGFの抑制が弱まる環境も想定されている.黄斑色素が減少すると,酸化ストレスを受けやすくなる.また喫煙は酸化ストレスを助長しているとされる.
❼ H因子:インヒビターとして補体経路を制御している. 補体系 制御(抑制)因子のH因子によく見られる単一ヌクレオチド多型(Y402H)は加齢黄斑変性と相関があり,補体経路の異常活性の環境に原因がある.補体経路の活性化は,炎症誘発因子・血管新生因子等の放出,組織損傷につながる.
- 加齢黄斑変性(広義.後期加齢黄斑症 late ageⲻrelated maculopathy
➀ 滲出型 wet type または exudative type/新生血管型
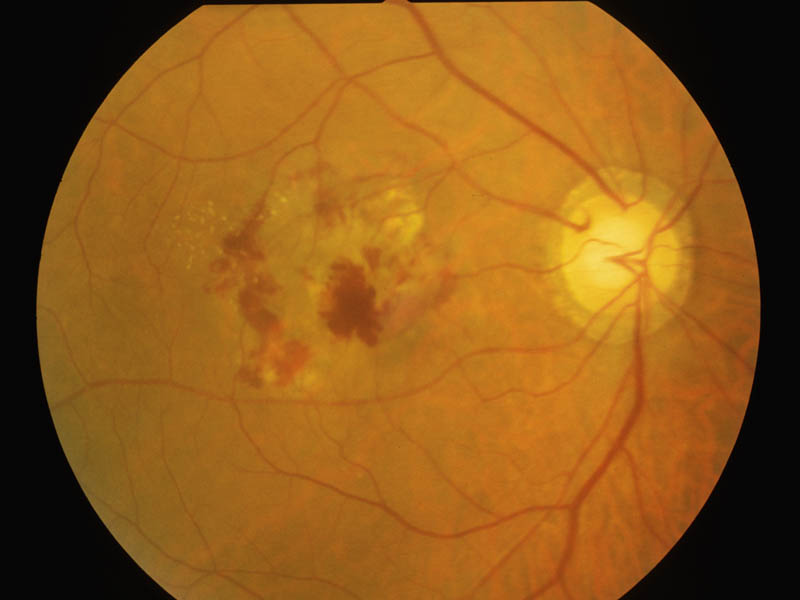
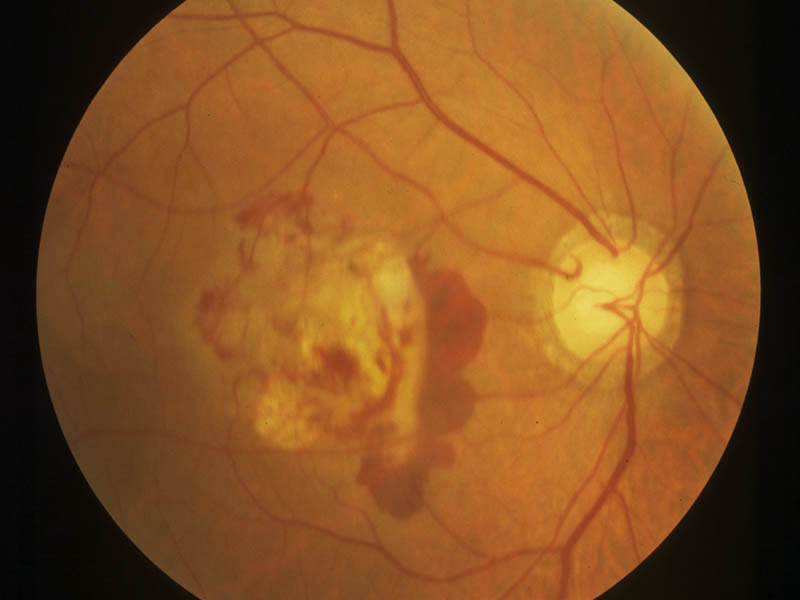
通常,加齢黄斑変性といえば本症(狭義)のことで,脈絡膜新生血管(choroidal neovascularization;CNV)が本態である(新生血管黄斑症).ドルーゼンや網膜色素上皮剝離に反応して脈絡膜毛細血管から発生した新生血管は,Bruch膜と網膜色素上皮を越えて感覚網膜に向かって拡大し,出血・浮腫を繰り返し,線維性増殖が進行する.経過中,大型の網膜色素上皮剝離や漿液性網膜剝離を伴う.増殖した血管結合織(肉芽組織)は最終的に線維成分が多くなり,瘢痕期病巣となる.
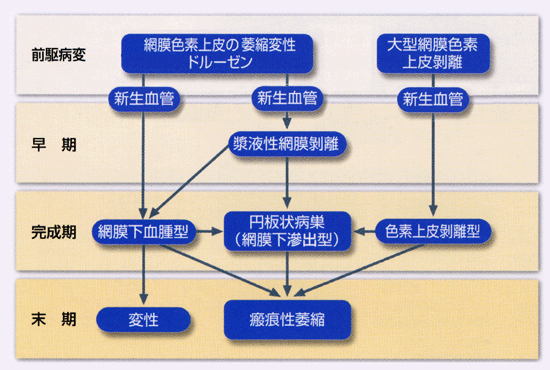
一般に,初期から強い変視症があり,進行するにつれ高度な中心暗点による視力障害をきたす.
➁ 萎縮型 dry type
脈絡膜血管が透見できる径250µm 以上の病巣で,網膜色素上皮・視細胞・脈絡膜毛細血管の萎縮性変化,ドルーゼンの成れの果てを含むBruch膜の肥厚・変性に伴う萎縮病態である.地図状萎縮 geographic atrophy と表現される.萎縮の前段階として,多量のリポフスチン貯留が危険視されている.これによりFAFでは色素上皮の状態により,過蛍光~低蛍光の混在所見となり,進行予測などの情報として注目されている.
他に原因疾患が確認されるか,網膜色素上皮裂孔や萎縮からCNVを生じたものなどは除外となる.
③ 滲出型:萎縮型 = 3:1
- 滲出型加齢黄斑変性(広義)
滲出型加齢黄斑変性(狭義 Gass分類
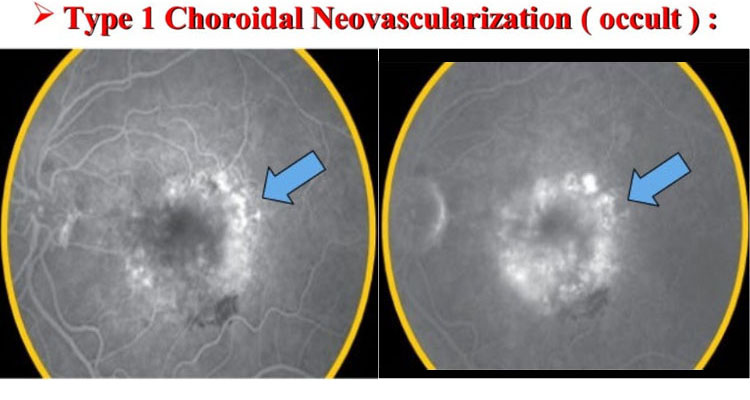
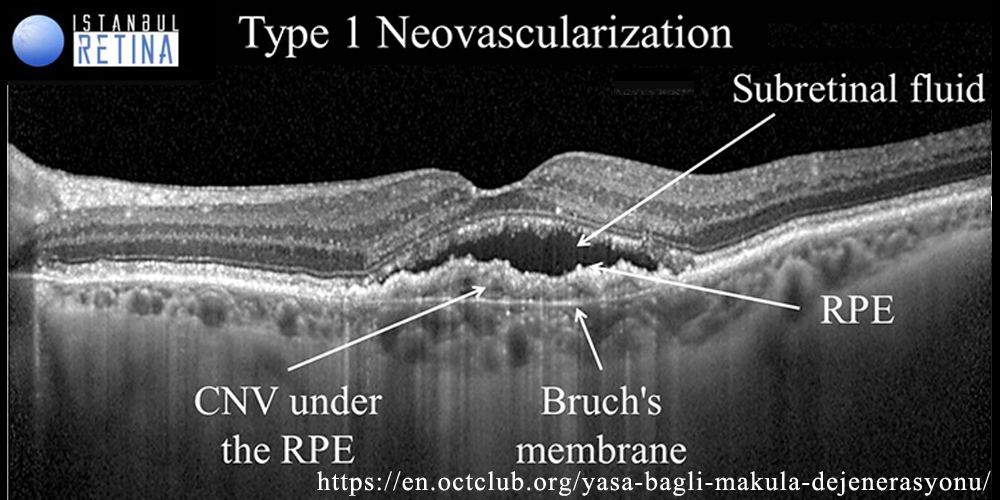
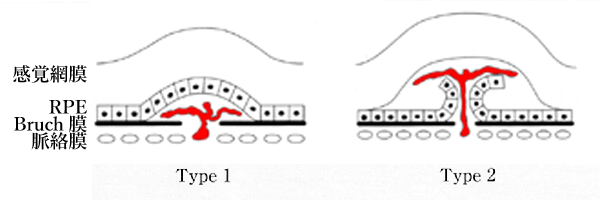
ⓐ Ⅰ型:RPE下のCNV
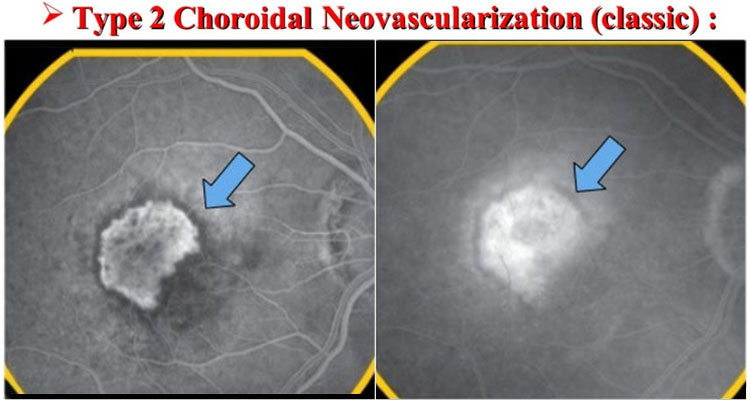
ⓑ Ⅱ型:RPEを超えたCNV蛍光造影所見では(参照:https://www.slideshare.net/MohamedELShaf3y/cnv-updates
ⓐ occult CNV:淡い(illⲻdefined)過蛍光
A:Early stages are poorly delineated with fluorescein.
B:Late stages are stained with irregular margins.
ⓑ classic CNV:旺盛な(wellⲻdefined)漏出
A:Early fluorescein angiogram its seen as well delineated vascular pattern.
B:Late stages it stained with indistinct margins.
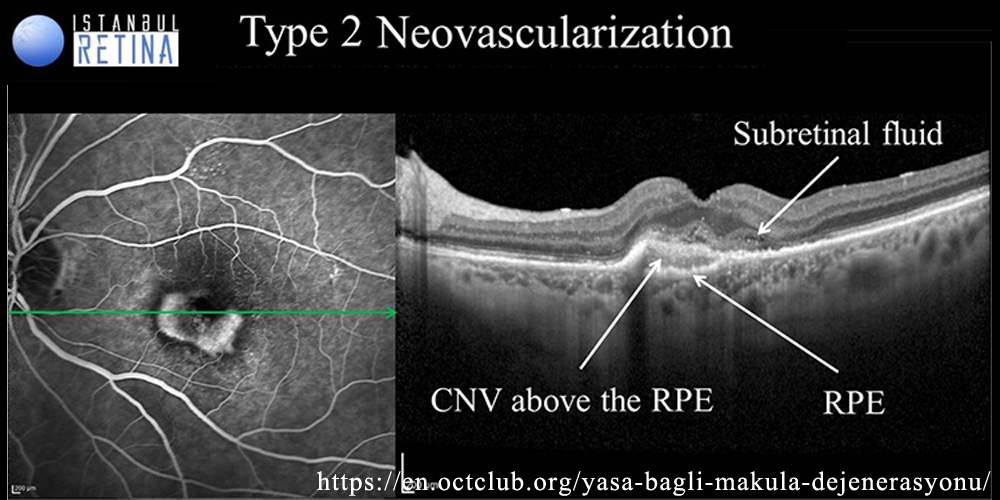
-
特殊型(非定型
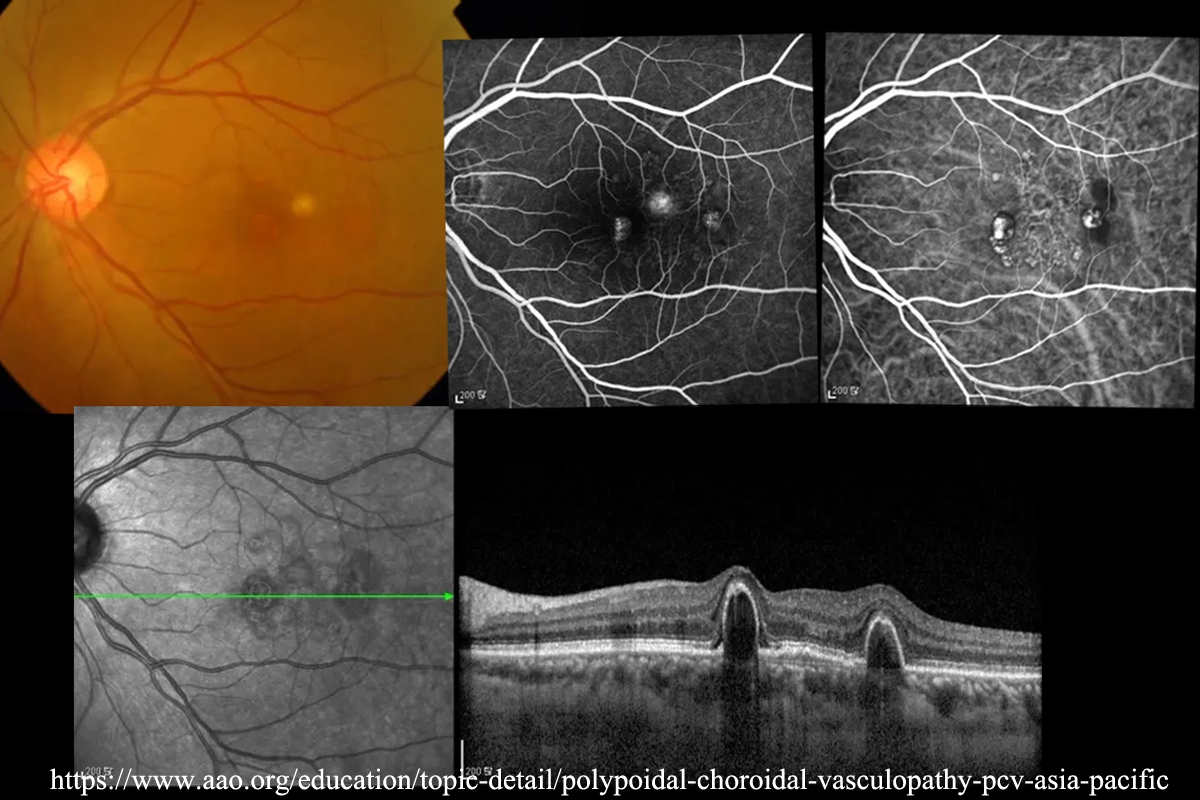
ⓐ PCV(polypoidal choroidal vasculopathy):脈絡膜内層に於いて, 異常血管網の終末部が拡張しpolypoidalポリープ状CNVを形成する.CNV(polyp)の主座は網膜色素上皮(RPE)裏面・Bruch膜内であることから, OCTでは,新生血管網は double layer sign として,ポリープ状病巣は急峻な RPE隆起 として描出される.ポリープ部は透過性亢進が強く,網膜色素上皮剝離(PED)を高率に合併する.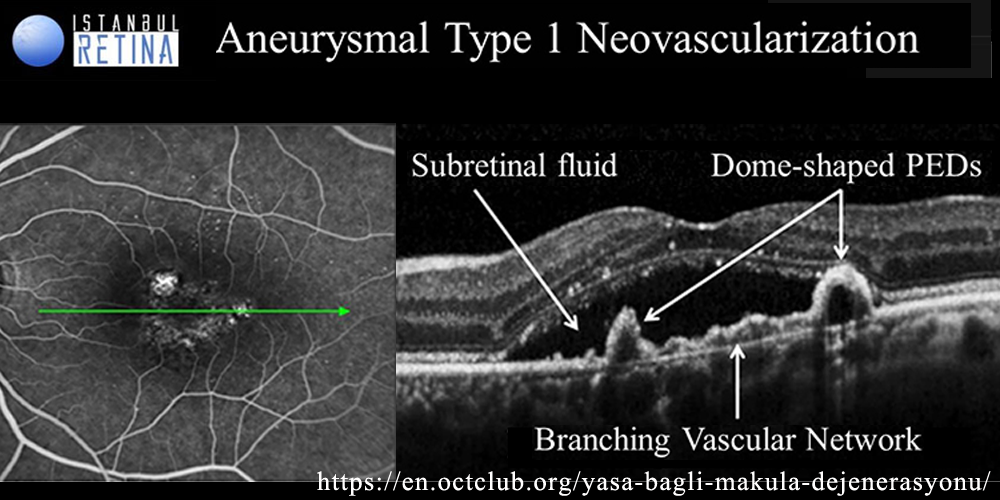
病理組織によりポリープ本体は type I の変形・成熟した血管壁であることが証明されている.ドルーゼンを前駆病変としない本パターンはアジア人 ∕ 男性に多いことが分かり,特殊型とは言えなくなっている(アジア型).
前駆所見として, 肥厚脈絡膜 が指摘されている.萎縮した脈絡毛細管板における虚血が新生血管の誘発になるとされる.※ double layer sign は,一般的に type I新生血管のOCT画像所見である.
※ 下方ぶどう腫や網膜色素線条に合併する脈絡膜新生血管にPCV型が多く,二次性PCVとも呼ばれている.
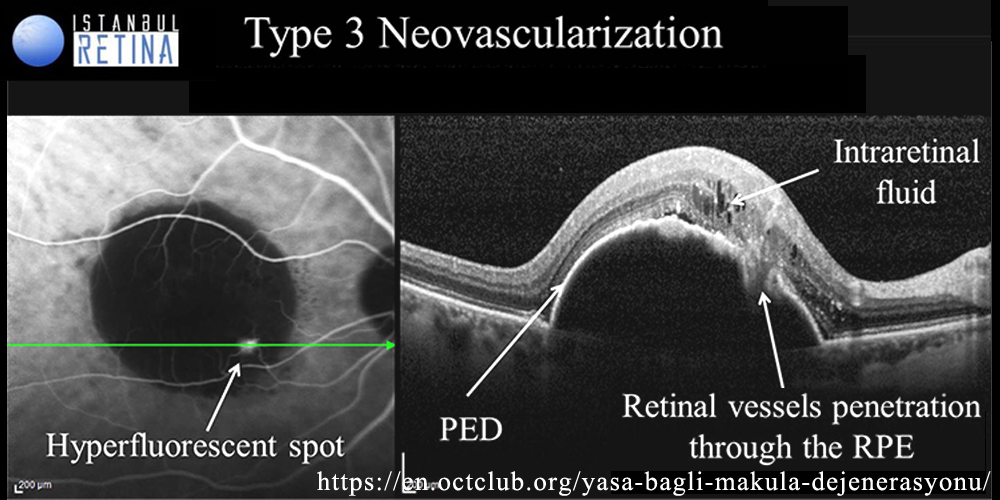 ⓑ RAP(retinal angiomatous proliferation):網膜内新生血管と脈絡膜血管の交通.AMD の type IIIと記載されることもある.OCTでは両者の交通部がRPEの断裂像として描出される.bump signである.
菲薄脈絡膜 との関連が指摘されている.
reticular pseudodrusen を伴うことが多い.
ⓑ RAP(retinal angiomatous proliferation):網膜内新生血管と脈絡膜血管の交通.AMD の type IIIと記載されることもある.OCTでは両者の交通部がRPEの断裂像として描出される.bump signである.
菲薄脈絡膜 との関連が指摘されている.
reticular pseudodrusen を伴うことが多い.
高齢女性に多く,しばしば両眼性である.
オリジナルは網膜から脈絡膜の方へ伸展する病態を説明している.
stage I は網膜内新生血管網の発生(intraretinal neovascularization) , stage II は網膜下への伸展(subretinal neovascularization) , stage III は脈絡膜新生血管(choroidal neovascularization)が発生し,網膜-脈絡膜の吻合となる.しかし,網膜内新生血管と脈絡膜新生血管の発生順は研究者の間で決着がない ? ようでもある.
新生血管部の網膜は脈絡膜のほうへ食い込むような形態を示す(通常の AMD では網膜を持ち上げるように進行する点で対照的)との説明もある. -
病型・治療方針・予後等に関連して,滲出型ではサブタイプ(亜型)としての考え方が推奨されている(日眼ガイドライン,2012).
➊ 典型滲出型加齢黄斑変性
➋ ポリープ状脈絡膜血管症(PCV
➌ 網膜内血管腫状増殖(RAP -
脈絡膜新生血管発生の基盤として端的には,
ドルーゼンを基に進行するのが典型滲出型加齢黄斑変性,肥厚脈絡膜を基に進行するのがポリープ状脈絡膜血管症,菲薄脈絡膜を基に進行するのが網膜内血管腫状増殖,という位置づけである. 【 各サブタイプ症例 】※ 本邦でのいわゆる広義滲出型加齢黄斑変性においては,ドルーゼンが少ないことが統計学的に明らかになっている.同時に肥厚脈絡膜の合併が多くなっている.
- 用語の変遷:OCTやFAFなど多様な検査が普及するにつれ細分化が余儀なくされている.
※MNV:macular neovascularization.網膜由来の新生血管もあるということで,脈絡膜ではなく黄斑新生血管と言おう,だとさ.
*type 1 MNV:RPE下にあるNV.PCVを含み,多様なPEDをきたす.
*type 2 MNV:RPEを超え網膜下に伸展したもの.
*type 3 MNV:網膜血管(深部血管網)から発芽し網膜外層へ向かうNV.脈絡膜循環と異常吻合をきたす.※新生血管があっても滲出性変化がない状態の AMD を含めて,新生血管型(neovascular)AMDということが推奨されている.
※「黄斑萎縮」は MNV の有無にかかわらず,境界明瞭な萎縮病巣に対して使用できる用語とされている.地図状萎縮や黄斑萎縮は、新生血管型 AMD の末期にみられる線維性瘢痕や嚢胞様黄斑変性に伴う網膜外層の萎縮性変化とは区別される.
- 用語の変遷:OCTやFAFなど多様な検査が普及するにつれ細分化が余儀なくされている.
老人性円板状黄斑変性(症 SDMD:senile disciform macular degeneration (Kuhnt᠆Junius)
かつて(1960年代後半!)英語病名が紹介された当初は,網膜下ないし脈絡膜上層を原発病巣とする遺伝的先天的な素因を有する病態を中心に考えられてきた.その後,新生血管周囲に網膜色素上皮細胞・線維芽細胞・膠原線維の増殖をきたした線維血管膜の形状を “円板(円盤)状 disciform”とし “老人性円板状黄斑変性症”と表現した.
しかし内容的にはかなり進行した,もしくはほとんど完成された瘢痕病態を意味するために,一方では “老人性”という表記を避ける傾向もあり,現在ではほとんど使わない.